Регуляция экспресии
Регуляция экспресии
Белковые домены связывающие ДНК
Инсуляторы
Интерференция РНК
Интерференция РНК – феномен, ведущий к посттранскрипционному молчанию генов (PTGS2).
Явление RNA interference (RNAi3) обнаружено Fire et al. в 1998 году у нематоды C.elegans. Было обнаружено, что введение двухцепочечной РНК (dsRNA1) в нематоду приводит к замолканию генов гомологичных введеной
dsRNA1 и образование малых РНК (siRNAs4). Позже выяснилось, что этот феномен широко распространен среди большинства организмов, включая простейших, животных и растений. Интерференция РНК заключается в разрезании dsRNA1 на короткие, ~20 нуклеотидов, фрагменты, которые выполняют роль матрицы для узнавания комлементарных РНК и разрезания их на фрагменты.
Механизм RNAi3 заключается в расщеплении двухцепочечной РНК на 21-23 пн фрагменты, которые действуют как матрица для разрушения гомологичных последовательностей РНК. Причем было установлено, что длинные dsDNA более активны чем короткие.
Попавшая в клетку dsRNA1 узнается белком Dicer, осуществляющим разрезание длинных
двухцепочечных РНК на короткие фрагменты. Далее такие дуплексы РНК с 2-3 нуклеотидными липкими концами, полученные Dicer связываются с белковым комплексом RISC (RNA-induced silencing complex), осуществляющим разрезание комплементарных одноцепочечных РНК в месте узнавания, что исключает трансляцию этих РНК. РНК разрезается в середине места узнавания, примерно 12 пн от 3'конца siRNA4. Эта позиция соответствует одному обороту двуцепочечного дуплекса РНК разрезающей и РНК которая разрежется. Вирусный белок Hc-Pro ингибирует действие комплеков RNAi3. (рис1.).
Dicer - АТФ-азная рибонуклеаза - инициатор сайленсинга, разрезает исходную dsRNA1, для матрицы. Имеется геликазный домен, С-концевой сегмент связывания с РНК и РНКазныйIII. Мышиный Dicer М=215 кДа и длиной 1373 аминокислоты расположен на конце 12 хромосомы и экспрессируется в различные фазы развития от эмбриональной
до взрослого состояния. Человеческий Dicer имеет массу 218 кДа.
RISC - мультибелковый комплекс ~500кДа, состоящий из нуклеиновых кислот и белков. Одна из субъединиц - Argonaute-2.
Длина некоторых интронов после процесcинга составляет ~20 нуклеотидов, что может указывать на участие их в механизме RNAi3.
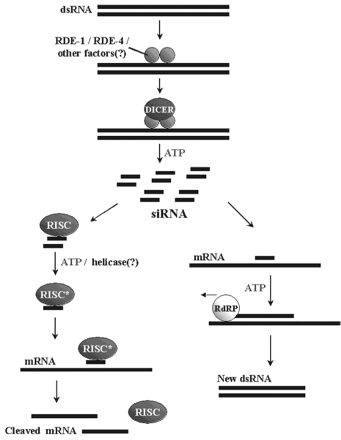
рис1. dsRNA1 проникшая в клетку узнается Dicer при помощи вспомогательных факторов RDE-1, RDE-4 и разрезается на фрагменты ~20 пн. siRNAs44. Фрагменты связываются с белковым комплексом RISC, который узнает и разрезает мРНК. Оставшийся одноцепочечный фрагмент может связываться с мРНК и служить затравкой для РНК-зависимой РНК-полимеразы (RdRP), которая достраивает мРНК до двухцепочечного
состояния, которое вновь узнается белком Dicer. И так происходит до тех пор, пока вся чужеродная мРНК не уничтожится. (Bantounas at al., 2004)
Защита от вирусов.
Интерференция РНК служит для защиты от проникновения в клетку молекулярных паразитов, таких как геномная РНК некоторых вирусов, состоящая из двух антипараллельных молекул. При запуске механизма RNAi3 такие дуплексы служат матрицей для последующего разрушения молекул РНК, с которых будут синтезированы вирусные белки. Однако вирусы не стояли на месте и приобрели способность противостоять клеточной защите. Вирусный белок Hc-Pro ингибирует работу белковых комплексов вовлеченных в механизм RNAi3.
Контроль активности транспозонов.
Так же RNAi3 служит для контролирования активности мобильных элементов. Мобильный элемент, или транспозон, это участок внутри ДНК какого-либо организма способный к копированию самого себя и встраиванию в любую часть генома. Если бы все транспозоны в клетке находились в активном состоянии они начали бы беспорядочно встраиваться в некодирующие участки генома, что может быть не так страшно, и в кодирующие участки, что неминуемо привело бы к нарушению работы генов и гибели организма. Предполагается, что механизм RNAi3 препятствует активации транспозонов и расселению их по геному. Таким образом, взаимодействие RNAi3 и транспозонной активности участвует в формировании структуры геномов большинства организмов. Считается, что транспозоны могут быть предками ретровирусов встроившихся когда-то в геном и существующими как внутренние паразиты. Из вышесказанного следует, что RNAi3 служит защитой
как с внешней стороны - вирусы, так и с внутренней - транспозоны.
Метилирование ДНК
RNAi3-зависимое метилирование ДНК - известный феномен у растений. Ранние наблюдения специфического метилирования ДНК, зависящего от репликации РНК, у растений описаны Wessenegger et al. (1994). Эта работа демонстрирует, что метилируются короткие районы ~30 пн, когда присутствует гомологичная РНК. При действии вирусного белка Hc-Pro, ингибирующего RNAi3, метилирование районов уменьшается. При метилировании ДНК, способность присоединять гистон ацетилазу уменьшается, что мешает разрыхлению хроматина и, соответственно, транскрипции генов. Модификации ДНК, полученные таким образом, могут наследоваться и передаваться дочерним клеткам, что может явиться механизмом клеточной памяти и регуляции развития организма.
Использование
в исследованиях.
Интерференция РНК используется исследователями для анализа функций различных генов. Если необходимо исключить из клетки какой-либо белок или несколько белков, исследователь может инъецировать двуцепочечные фрагменты РНК, комплепментарные участку мРНК, и механизм RNAi3 удалит мРНК и предотвратит их трансляцию. Это можно проделывать на различных этапах клеточного цикла. Такой подход называется генным нокдауном. Например, таким способом было систематически инактивировано 5690 генов C.elegans для определения генов, регулирующих продолжительность жизни. В результате эксперимента был обнаружен ген митохондриальной лейцил-тРНК-синтетазы и показано, что мутации этого гена остлабляют работу митохондрий и увеличивают продолжительность жизи. Было предположено, что это результат уменьшения уровня АТФ и потребления кислорода. Введение конструкций, экспрессирующих РНК, содержащую инвертированные повторы. Такой механизм, вероятно, может происходить и в
естественных условиях.
Лечение заболеваний.
Существует два основных нарушения при развитии рака. Первое, это нарушение клеточного цикла, результатом которого является ненормальный рост клеток, и второе это потеря чувствительности к белкам вызывающим апоптоз, или клеточную смерть.
RNAi3 может быть использована для лечения рака. Для этого можно создать нокдаун генов ответственных за клеточный цикл и противоапоптозных генов в клетках опухоли. Для избирательного действия на раковые клетки можно использовать RNAi3, вводя уникальные последовательности dsRNA1, специфичные для какого-нибудь определенного гена, или вводя их непосредственно в опухоль.
Недавние исследования ясно показали продвинутость метода RNAi3 в подавлении роста и разрушении раковых клеток. Предпринимаются успешные попытки
введения вирусных векторов в раковые клетки, что так же способствует подавлению их роста. Однако все эти методы лечения находятся пока на предклинических испытаниях.
Болезни, вызванные вирусами и бактериями, продолжают являться основной причиной смертности людей в мире и продолжают вызывать беспокойство возможностью появления новых форм опасных заболеваний и использование их террористами. В настоящее время ВИЧ достиг эпидемических показателей в африканских странах и продолжает являться важной причиной смертности среди гомосексуалистов и наркоманов.
Способность RNAi ингибировать репликацию вирусов и других инфицирующих агентов была продемонстрирована на клеточных культурах и подает надежды на лечение этих заболеваний.
- Fire, A., Xu, S., Montgomery, M.K., Kostas, S.A., Driver, S.E., and Mello, C.C. 1998. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature 391: 806-811
- Sharp RNA interference-2001 Genes and Development Vol. 15, No. 5, pp. 485-490, March 1, 2001
- S. Mattick, M.J. Gagen The Evolution of Controlled Multitasked Gene Networks: The Role of Introns and Other Noncoding RNAs in the Development of Complex Organisms John Molecular Biology and Evolution 18:1611-1630 (2001)
- I Bantounas, L A Phylactou and J B Uney RNA interference and the use of small interfering RNA to study gene function in mammalian systems Journal of Molecular Endocrinology (2004)
Энхансеры и супрессоры
Энхансеры - участки вне промотора, которые связываются с различными факторами транскрипции и способны усиливать транскрипцию определенных генов.
Энхансеры могут располагаться в облости от промотора до 10000 пн от него (энхансер SV40) перед, после промотора или пределах интрона.
Некоторые гены контролируются более чем одним энхансером (Drosophila even-skipped ген)
Регуляторные элементы дрожжей S.cerevisae называются UAS (upstream activating sequences) функционально схожи с энхансерами высших эукариот. Большинство генов S. cerevisae имеют один UAS, который лежит в пределах нескольких сотен пн от кэп-сайта промотора.