Репарация ДНК
Репарация ДНК
Общие сведения
Агенты повреждающие ДНК
Излучение
1. ионизирующая радиация (гамма лучи, рентгеновские лучи)
2. Ультрафиолетовое излучение (особенно ~260 нм, именно в этой области происходит максимальное поглощение ДНК)
Активные радикалы кислорода образуемые во время нормального клеточного дыхания в различных биохимических путях.
Химические вещества окружающей среды.
Многие углеводороды.
Химикаты используемые в противоопухолевой химотерапии.
Типы повреждений ДНК
1. Все четыре основания в ДНК (A, T, C, G) могут быть ковалентно модифицированы в различных положениях.
Наиболее частое - это потеря аминогруппы (дезаминирование) — в таком случае C превращается в U.
Неправильное включение оснований происходящее из-за ошибок в работе ДНК полимераз при репликации.
Наиболее часто происходит включение урацила вместо тимина.
Нарушения структуры.
В ДНК могут происходить разрывы. Разрывы могут быть одноцепочечные, или могут разорваться обе цепи ДНК.
Ионизирующая радиация может быть частой причиной таких разрывов.
Между соседними основаниями может образоваться ковалентная связь, причем связь может образоваться между соседними основаниями в одной цепи или между двумя цепями ДНК.
типы повреждения ДНК
изменение одного основания
апуринизация
замена С на У
замена А на гипоксантин
алкилирование основания
вставка или делеция нуклеотида
встраивание аналогичного основания
изменение двух оснований
образование тиминовых димеров
поперечная связь с бифункиональным алкилирующим агентом
разрушение цепи
ионизирующее излучение
радиоактивное разрушение элементов остова
поперечные связи
между основаниями одной нити или двух параллельных нитей
между ДНК и белковыми молекулами, например гистонами
Репарация поврежденных оснований
Поврежденные основания могут быть исправлены различными путями:
Прямое химическое исправление повреждений.
Эксцизионная репарация (ER), при которой поврежденное основание удаляется и заменяется новым. Имеется три модели эксцизионной репарации, в каждой из которых используется свой собственный набор ферментов.
Эксцизионная репарация оснований (BER).
Эксцизионная репарация нуклеотидов (NER).
Мисмэтч репарация(MMR).
Прямое исправление повреждений.
Наиболее частая причина точечных мутаций у человека - это спонтанное добавление метильной группы - один из типов алкилирования. Такие модификации исправляются ферментами называемыми гликозилазами, исправляющими ошибку без разрушения цепи ДНК.
Некоторые препараты используемые в химотерапии также повреждают ДНК путем алкилирования.
Проблема репарации состоит в том, что ограниченным набором ферментов и механизмов клетка должна справиться со многими повреждениями вызванными самыми различными химическими и физическими агентами.
Эксцизионная репарация оснований (BER)
Основные ключевые события:
1. Удаления поврежденного основания (происходит ~ 20,000 раз в день в каждой клетке человеческого тела) ДНК гликозилазими. У человека имеется по крайней мере 8 генов кодирующих различные ДНК гликозилазы, кадждые из которых распознают свой набор повреждений оснований.
2. Удаление дезоксирибофосфата приводит к образованию пустоты в ДНК.
3. Замена правильным нуклеотидом. Это функция у человека выполняется ДНК полимеразой бетта.
4. Лигирование разрыва цепи. Имеется два фермента, оба нуждаются в АТФ.
Эксцизионная репарация нуклеотидов (NER)
NER отличается от BER несколькими путями.
Использованием различных ферментных систем.
Даже если ошибка в одном нуклеотиде, удаляется сразу множество нуклеотидов в районе повреждения.
Основные ключевые события NER:
1.Повреждение распознается одним или несколькими факторами связывающимися с местом повреждения.
2. ДНК раскручивается в месте повреждения. В этом процессе участвуют
различные транскрипционные факторы IIH, TFIIH, (которые так же работают при нормальной транскрипции).
3. Разрез ДНК происходит с 3' и 5'-конца от повреждения, в результате чего удаляется фрагмент ДНК содержащий поврежденный нуклеотид.
4. Новая цепь ДНК достраивается по матрице неповрежденной цепи ДНК полимеразами дельта или эпсилон.
5. Лигазы сшивают вновь синтезированный конец цепи.
Пигментная ксеродерма (XP)
XP редкое наследственное заболевание человека проявляющееся в поражении кожи при облучении светом, что в конечном итоге приводит к развитию рака кожи и гибели больного.
Болезнь возникает из-за мутаций в генах участвующих в NER репарации. Например:
XPA кодирует белок связывающийся с местом повреждения и помогающий сборке репарирующего комплекса.
XPB и XPD, которыя являются частями транскрипционного фактора TFIIH. Некоторые мутации в XPB и XPD также могут являться причиной преждевременного старения.
XPF разрезает цепь ДНК с 5'-конца от повреждения.
XPG разрезает цепь с 3'-конца.
Мисмэтч репарация(MMR)
Мисмэтч репарация исправляет ошибочно встроенные неповрежденные основания которые не образуют нормальное Уотсон-Криковское спаривание (A•T, C•G). Такие ошибки происходят во время работы ДНК полимеразы при репликации.
В мисмэтч репарации участвуют ферменты вовлеченные как в BER, так и в NER репарацию, так и специализированные ферменты.
Синтез ДНК при мисмэтч репарации осуществляется ДНК полимеразами дельта или эпсилон.
Система мисмэтч репарации участвует в увеличении точности рекомбинации при мейозе.
Репарация разрывов ДНК
Ионизирующая радиация и некоторые химические вещества способны разорвать одну или две цепи ДНК.
Одноцепочечные разрывы (SSB)
Разрывы одной из цепей ДНК часто исправляются ферментами участвующими в BER репарации.
Двуцепочечные разрывы (DSB)
Имеется два механизма которые способны устранить двуцепочечных разрывов ДНК:
Прямое соединение сломаных концов. Этот процесс требует специальных
ферментов, которые узнают и связывают разорванные концы с последующим их сшиванием. Если разорванная ДНК имеет тупые концы и соединение двух фрагментов ДНК происходит случайно, то такая репарация называется NHEJ. Белок Ku необходимый для NHEJ. Ku - гетеродимерная субъединица, состоящая из двух белков Ku70 и Ku80.
Ошибки возникающие при прямом присоединении могут являться причиной транслокаций.
Полинуклеотидлигаза – восстановл. одноцеп. разрывы ДНК
Гомологичная рекомбинация
Гомологичная рекомбинация способна восстанавливать поломанные концы хромосом используя ДНК не поврежденной сестринской хроматиды доступной после удвоения хромосом.
Гены необходимые для гомологичной рекомбинации - BRCA-1 and BRCA-2.
Конверсия гена
Донором нового гена может быть:
гомологичная хромосома (во время мейоза)
систринская хроматида (так же во время мейоза)
дуплицированный ген той же хромосомы (во время митоза)
Исправление ошибок за счет 3’-5’ экзонуклеазной активности полимеразы при репликации (только у прокариот) (мутация E.coli mutD-мутатор-измен. -субъединицы ДНК-пол.III)
Тиминовые димеры, фермент фотолиаза ген-phr (у низших эукариот)
Удаление присоединенных алкильных и метильных групп - O-6-метилгуанинтрансфераза (ген ada)-удаляет О-6-метилгуанин
эксцизионная р. оснований [Е.coli ] [человек | узнавание поврежд. XPA-белком в ассоциации с RPA | привлекается ф-р транскр. TFIIH (P52, Р34, Р44, Р62, XPB-XPD-геликазн. акт-ть) | ERCC1-XPF, XPG – нуклеазы, надрезають ДНК по обе стороны от поврежд. | ДНК-полимераза- и вспомогат. белки RFC и PCNA застраивают брешь]
р. азотистых осн.-гликозилаза удаляет осн.
AP-сайт (апуриновый, апиримидиновый) | AP-эндонуклеаза опознает брешь, разрез. 5’-ДНК
пострепликативная р. (ПРР)
SOS-р. белки соед. с ДНК-полимеразой, доч. ДНК строится напротив поврежд. ДНК
Сокращения.
BER - Base Excision Repair
NER - Nucleotide Excision Repair
MMR - Mismatch Repair
NHEJ - Nonhomologous End-Joining
Мисмэтч репарация
В процессе реплакации, в результате ошибок полимеразы, могут встраиваться некомплиментарные нуклеотиды, что может привести к мутациям в дочерней цепи ДНК. Неспареные основания узнаются ферментами мисмэтч репарации и осуществляют замену ошибочно спаренных нуклеотидов.
Ферменты данной системы обеспечивают гомологичную рекомбинацию, а также задержку клеточного цикла в ответ на повреждения ДНК.
Система репарации ошибочно спаренных нуклеотидов у E. coli, использующая белки MutHLS, распознает и репарирует все некомплементарные пары оснований за исключением C–C. Кроме того, эта система репарирует небольшие вставки в одну из цепей ДНК, образующиеся в результате ошибок репликации, длина которых не превышает четырех нуклеотидов.
Обычно у E. coli ДНК метилирована Dam-метилазойпо сайтам GATC. Однако после завершения репликации дочерняя цепь ДНК некоторое время остается неметилированной.
Эта система может быть реконструирована in vitro с использованием
ДНК с одной метилированной цепью в качестве субстрата, к которой добавляются очищенные белки MutH, MutL, MutS, UvrD (хеликаза II), холофермент ДНК-полимеразы III, ДНК-лигаза, белок SSB, а также одна из экзонуклеаз: ExoI, ExoVII или RecJ. Процесс репарации инициируется внесением одноцепочечного разрыва в неметилированную цепь вблизи частично метилированного сайта GATC с последующим гидролизом цепи ДНК и заполнением образующейся одноцепочечной бреши. При этом белок MutS связывается с ошибочно спаренными нуклеотидами. У белка MutL не обнаружено ферментативной активности, хотя он взаимодействует с MutS и необходим для активации MutH – эндонуклеазы, осуществляющей одноцепочечный разрыв ДНК. Таким образом, комплекс MutS–MutL, собранный на участке ДНК с ошибочно спаренным нуклеотидом, стимулирует эндонуклеазную (никазную) активность MutH. Бесклеточная система не требует присутствия MutH при наличии в ДНК-субстрате одноцепочечного разрыва. MutHLS-система репарации может
использовать частично метилированные последовательности GATC, расположенные выше и ниже поврежденного участка ДНК. При этом в
вырезании ошибочно включенного нуклеотида помимо хеликазы II принимает участие одна из экзонуклеаз: ExoI (3’-экзо), ExoVII (3’- и 5’-экзо) или RecJ (5’-экзо) в зависимости от расположения GATC-сайта по отношению к корректируемому нуклеотиду. Вслед за вырезанием нуклеотида образовавшаяся одноцепочечная брешь заполняется холоферментом ДНК-полимеразы III в присутствии SSB-белка и ДНК-лигазы. Следует подчеркнуть, что использование белка MutH и Dam-метилазы для распознавания дочерней цепи реплицировавшейся ДНК является уникальным свойством грамотрицательных бактерий. У грамположительных бактерий не происходит метилирование цепей ДНК в целях маркировки. Если сайты GATC полностью метилированы, MutHLS-система репарации E. coli изменяет ошибочно спаренные нуклеотиды в обеих цепях ДНК с одинаковой эффективностью.
У E. coli существуют, по крайней мере, еще два специфических
пути репарации ошибочно спаренных нуклеотидов. Система VSP (very short patchrepair pathway) репарирует некомплементарные пары G–T, заменяя их на G–C. Считается, что такие пары образуются в результате дезаминирования 5-метилцитозина в сайтах, где остатки С метилированы Dcm-метилазой. С более низкой эффективностью эта же система заменяет пары G–U на G–C. Другая MutY-зависимая система репарации специфически ликвидирует последствия окислительных повреждений гуанина. Если dGTP окисляется с образованием 8-оксо-dGTP, белок MutT расщепляет последний, предотвращая его включение в ДНК. Если же он все-таки включается напротив остатка С, то Fpg-гликозилаза (MutM) удаляет это модифицированное основание. В том случае, когда 8-оксо-G остается в составе ДНК, в следующем раунде репликации он спаривается с А, и в итоге может произойти трансверсия G–C>T–A. В этом случае белок MutY действует как ДНК-гликозилаза, удаляющая остаток A из некорректной пары, и как AP-лиаза, вносящая одноцепочечный
разрыв по соседству с AP-сайтом. Далее следуют процессы, уже рассмотренные выше в связи с функционированием системы репарации BER. Последовательность реакций с участием MutY также репарирует некомплементарные пары A–G и A–C с образованием соответственно пар C–G и G–C. Репарация ошибочно спаренных оснований у эукариот происходит при
участии комплекса белков, подобного системе MutHLS бактерий. Белок GTBP человека представляет собой гомолог бактериального белка MutS, а у дрожжей в соответствующей роли выступает белок Msh6. Распознавание ошибочно спаренных нуклеотидов у человека осуществляется гетеродимером MSH2–GTBP. Гомологами MutL в клетках S. cerevisiae являются белки MLH1 и PMS2, которые также существуют в виде гетеродимерных комплексов. Мутации в генах, кодирующих эти белки у человека, сопровождаются формированием мутаторного фенотипа и развитием наследственного неполипозного рака кишечника (синдром HNPCC – hereditary nonpolyposis colon cancer).
Прямая репарация
Существуют два основных пути репарации алкилированных оснований: эксцезионная репарация оснований (BER) и прямая репарация поврежденных оснований. При BER DNA-гликозилазы выщепляют цитотоксичные алкилированные основания в DNA на первом шаге с образованием AP-сайта и последующим его процессированием.В случае прямой репарации реализуются два способа: репарация алкилтрасферазами либо окисление алкильной группы, в обоих случаях происходит регенерация неповрежденных оснований. Если протекает репарация алкилтрасферазами (у млекопитающих только O6-алкилгуанин репарируется по этому пути), то O6-алкилгуанинтрансфераза (AGT) переносит метильную или этильную группу с O6-алкилгуанина на один из собственных остатков цистеина. Алкилированный в результате собственной активности белок инактивируется, но может служить регулятором активности своего гена и нескольких других. В отличие от суицидных O6-метилгуанинтрансфераз, направленно деметилирующих высокомутагенное и токсичное
повреждение O6-метилгуанин, AlkB из E. coli и его человеческие аналоги hABH2 и hABH3 окисляет метильные группы 1-метиладенина (1-meA) и 3-метилцитозина (3-meC) в DNA для регенерации немодифицированных оснований аденина и цитозина.
O6-алкилгуанинтрансфераза
O6-алкилгуанинтрансферазная активность обнаружена у большинства организмов и препятствует мутагенному действию O6-алкилгуанина. AGT превращает O6-алкилгуанин в гуанин, перемещая алкильную группу с DNA на реакционный остаток цистеина в белке в ходе необратимой реакции.
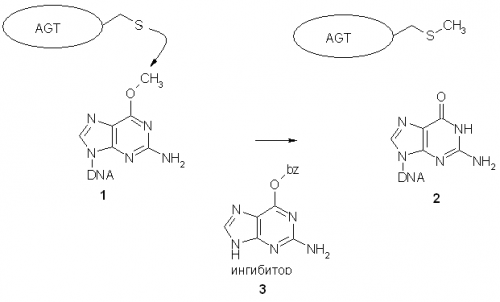
Такое ковалентное присоединение алкильной группы к остатку цистеина инактивирует фермент. Поэтому AGT - суицидный фермент, который подвергается протеолитической деградации после одной
реакции трансалкилирования. Структурные исследования позволяют обнаружить, что активный центр AGT расположен в объеме фермента на некотором расстоянии от DNA-связывающего участка. Считается, что фермент "работает" по механизму "переворачивания нуклеотида", чтобы плотно сблизить основание субстрата и нуклеофильный активный центр AGT.
Важность AGT в защите млекопитающих от токсического и мутагенного эффектов алкилирующих агентов была продемонстрирована на мышах. Трансгенные мыши с чрезмерной экспрессией AGT проявляют значительно более низкий уровень возникновения опухолей в ответ на действие метилирующего агента - N-метил-N-нитрозомочевины, в то время как мыши с дефицитом AGT оказывались на много более восприимчивы к инициированию опухоли и токсическим эффектам этого агента по сравнению с немутантными мышами. AGT - важный фермент в противоопухолевой терапии так как он препятствует цитотоксическим эффектам противоопухолевых агентов класса хлороэтилнитрозомочевины (CENU), например
BCNU (N,N-бис(2-хлороэтил)N-нитрозомочевина) или темозоломид. Было показано, что количество, в котором присутствует AGT в опухолях, в основном определяет на сколько благоприятным окажется исход противоопухолевой терапии с использованием CENU. CENU первоначально взаимодействует с O6-карбонильной группой гуанина с образованием соединения 4, которое впоследствии преобразуется в N1,O6-этаногуанин 5. Соединение 5 перегруппируется в течение нескольких часов в физиологически активный ICL 6. AGT препятствует образованию 6 при взаимодействии с 4 или 5, возобновляя гуанин или формируя DNA-белковый аддукт 8. Экспериментально получено подтверждение образования аддукта 8, но он был выделен в слишком малом количестве для его детального описания. При биохимическом исследовании этой проблемы был введен N1,O6-этаноксантин
9 как стабильный аналог 5 в DNA. Этаноксантин 9 реагирует с AGT с образованием стабильного DNA-белкового аддукта 7. Этот подход позволил формировать ковалентно связанный AGT-DNA аддукт 10 в большом количестве, который может быть использован для определения структуры AGT связанного с DNA. Взаимовлияние AGT и алкилирующей терапии привело к поиску ингибиторов AGT, которые могут быть использованы в терапии рака в сопряжении с алкилирующими агентами. К настоящему времени созданы ингибиторы, главным образом, производные гуанина с заместителями в O6-позиции. O6-бензилгуанин 2 был обнаружен как типичный ингибитор AGT, с которым сравнивают новые молекулы. Эффективность O6-BzG в усилении цитотоксичности CENU продемонстрирована на моделях животных. Лимитирующим фактором этого терапевтического подхода является токсичность для здоровых органов, частично для костного мозга. Некоторые
группы ученых направлены обойти эту проблему путем генерирования ATG-варианта, устойчивого к ингибированию O6-BzG, что может быть использовано для защиты костного мозга при помощи генного переноса.


Оксидоредуктазы AlkB, hABH2 и hABH3
Еще один путь прямой репарации алкилированных оснований - окисление алкильной группы с регенерацией неповрежденного азотистого основания. Фермент AlkB у Escherichia coli и два человеческих аналога hABH2 и hABH3 направленно деметилируют 1-метиладенин и 3-метилцитозин в DNA. Но в отличие от AGT, эти ферменты обладают субстратной специфичностью, направленной на поверхность пар оснований G:C и A:T. Повреждения 1-алкиладенин
и 3-метилцитозин формируются когда аденин и цитозин находятся в одноцепочечной структуре (в период репликации или транскрипции) и являются субстратами для AlkB, hABH2 и hABH3. Они окисляют метильные группы 1-метиладенина (1-meA) и 3-метилцитозина (3-meC) в DNA для регенерации азотистых оснований аденина и цитозина. Было также показано, что AlkB защищает от токсичного повреждения - аддукта с этильной группой и преобразует 1-этиладенин в аденин в DNA, продуцирующий в результате реакции ацетальдегид. Таким образом репарируются повреждения известного мутагена и канцерогена этиленоксида, эндогенно образующегося в ходе метаболизма этилена, а также широко применяющегося как фумигант для стерилизации. Аддукты с гидроксиэтилом, генерируемые этиленоксидом обнаружены в DNA клетки. Другие малые алкилирующие эпоксиды также задействованы в большом количестве в химическом производстве. Было показано, что AlkB снижает токсические эффекты DNA-повреждающих агентов, генерирующих гидроксиэтильный,
пропильный и гидроксипропильный аддукты. AlkB репарирует алкилированные трифосфаты 1-me-dATP активно, но неэффективно. Предполагалось, что эта способность может снижать уровень встраивания алкилированных трифосфатов при синтезе DNA; к тому же Фрагмент Кленова DNA полимеразы I у E. coli может использовать 1-me-dATP как предшественник для синтеза DNA in vitro. Человеческие ферменты hABH2 и hABH3 также деметилировали 1-метиладениновые остатки в поли(dA), они были неэффективны на коротких субстратах. Таким образом hABH3 обладал очень низкой активностью на тримере d(Tp1-meApT), тогда как у hABH2 активности не было обнаружено.
AlkB и его человеческие аналоги является частью -кетоглутарат/Fe(II)-зависимого суперсемейства диоксигеназ, и в процессе репарации протекает свместно декарбоксилирование -кетоглутарата и окислительное деметилирование поврежденного основания. Повреждения 1-meA и 3-meC формируются в основном в одноцепочечной DNA и предположительно
возникают в репликативной вилке и в активно транскрибируемых генах где они могут заблокировать DNA- и RNA-полимеразы. В действительности AlkB, hABH2 и hABH3 репарируют эти повреждения в одноцепочечной DNA, но также протекает репарация олигонуклеотидов, отожженных с комплементарной цепью после алкилирования. Эффективность репарации 1-метиладенина AlkB не зависит от полинуклеотидной структуры, но необходимо наличие нуклеотид-5'-фосфатной группы. Также человеческие ферменты hABH2 и hABH3 деметилировали остатки 1-метиладенина в поли(dA), они были неэффективны на коротких субстратах. К тому же, повреждения, содержащие положительный заряд (рибонуклеозиды 1-meA и 3-meC имеют соответственно pKa= 9.3 и 9.6) лучше репарировались, чем незаряженные основания (1-meG и 3-meT). Однако, так как 1-meG (и в меньшей степени 3-meT) репарировались AlkB, то формальный положительный заряд основания не является необходимым условием для функционирования AlkB. С этой точки зрения
пока неясно, зависит ли этот результат от того, что положительно заряженные основания лучше распознаются посредством электростатических взаимодействий с AlkB или положительно заряженные основания просто делают DNA лучшей уходящей группой после гидроксилирования метильной группы.
Сокращения:
» Orlando D. Scharer (2003) Angew. Chem. Int. Ed. 42, 2946-2974
» James C. Delaney and John M. Essigmann Mutagenesis, genotoxicity, and repair of 1-methyladenine, 3-alkylcytosines, 1-methylguanine, and 3-methylthymine in alkB Escherichia coli
» Pertti Koivisto, Tod Duncan, Tomas Lindahl, and Barbara Sedgwick Minimal Methylated Substrate and Extended Substrate Range of Escherichia coli AlkB Protein, a 1-Methyladenine-DNA Dioxygenase*
» Duncan, T., Trewick, S. C., Koivisto, P., Bates, P. A., Lindahl, T. & Sedgwick, B. (2002) Proc. Natl. Acad. Sci. USA 99, 16660-16665. 5. Aas, P. A., Otterlei, M., Falnes, P. O., Vagbo, C. B., Skorpen, F., Akbari, M., Sundheim, O., Bjoras, M., Slupphaug, G., Seeberg, E., et al. (2003) Nature 421, 859-863.
» Hollis, T., Lau, A., and Ellenberger, T. (2000) Mutat. Res. 460, 201-210
» Daniels, D. S., and Tainer, J. A. (2000) Mutat. Res. 460, 151-163
» Trewick, S. C., Henshaw, T. F., Hausinger, R. P., Lindahl, T., and Sedgwick, B. (2002) Nature 419, 174-178
» Falnes, P. O., Johansen, R. F., and Seeberg, E. (2002) Nature 419, 178-181
» Duncan, T., Trewick, S. C., Koivisto, P., Bates, P. A., Lindahl, T., and Sedgwick, B. (2002) Proc. Natl. Acad. Sci. U. S. A. 99, 16660-16665
» Aas, P. A., Otterlei, M., Falnes, P. O., Vagbo, C. B., Skorpen, F., Akbari, M., Sundheim, O., Bjoras, M., Slupphaug, G., Seeberg, E., and Krokan, H. E. (2003) Nature 421, 859-863
» Aravind, L., and Koonin, E. V. (2001) Genome Biology 2, 0007.1-0007.8
» Bodell, W. J., and Singer, B. (1979) Biochemistry 18, 2860-2863
» Boiteux, S., and Laval, J. (1982) Biochimie (Paris) 64, 637-641
» Larson, K., Sahm, J., Shenkar, R., and Strauss, B. (1985) Mutat. Res. 150, 77-84
» Dinglay, S., Trewick, S. C., Lindahl, T., and Sedgwick, B. (2000) Genes Dev. 14, 2097-2105
Репарация разрывов ДНК
Фотореактивация
Абсорбция энергии УФ излучения молекулами ДНК приводит к образованию различных типов повреждений. Хотя одно- и двуцепочечные разрывы, а также ДНК-белковые сшивки могут возникать, большая часть индуцированных УФ-излучением повреждений приходится на модификацию азотистых оснований, с образованием циклобутан пиримидиновых димеров (CPD) и пиримидин-пиримидоновых фотопродуктов (6-4PP), как наиболее часто встречающихся типов фотоповреждений.
Пиримидиновые димеры являются ингибиторами и для репликации, и для транскрипции, что замедляет рост и приводит к мутагенезу в процессе репликации ДНК, если такие повреждения остаются неотрепарированными.
Для удаления индуцированных светом повреждений в ДНК у многих организмов применяются ферменты, специфично связывающиеся с CPD (CPD-фотолиаза) или с 6-4PP (6-4PP-фотолиазы) и исправляющие эти повреждения. CPD-фотолиазы обнаружены в бактериях, грибах, растениях, беспозвоночных и во многих позвоночных, 6-4PP-фотолиазы обнаружены, пока, только в Drosophila, тутовом шелкопряде, Xenopus laevis и в гремучих змеях, но не у Escherichia coli или дрожжей. У людей не обнаружено фотолиаз. Фотолиазы содержат FAD как каталитический кофактор и дополнительный хромофор в качестве светособирающей антенны.
Дополнительные хромофоры – это или 5,10-метенилтетрагидрофолат (MTHF), или 8-гидрокси-5-деазорибофлавин (8-HDF), с максимумами поглощений на длинах волн 380 и 440 нм, соответственно. Кристаллические структуры CPD-фотолиаз E.coli и Anacystis nidulans подтверждают, что для связывания с ДНК ферменты поворачивают пиримидиновый димер из дуплекса в углубление, содержащее каталитический кофактор. Затем циклобутановое кольцо расщепляется в ходе переноса, индуцированного светом электрона. CPD-фотолиазы селективно распознают CPD, подобно ДНК-связывающим белкам. Белый свет или UV-B-излучение индуцируют экспрессию CPD-фотолиаз. В отличие от CPD-фотолиаз, 6-4PP-фотолиаза стабильно экспрессируется и не регулируется ни белым светом, ни UV-B-излучением.
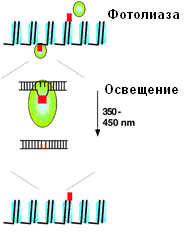
Схематичное изображение фотореактивации в хроматине. Октамеры гитонов голубого цвета, ДНК - черного. Фотолиаза связывается с циклобутан-пиримидиновыми димерами (CPD), поворачивает пиримидиновый димер и регенерирует природные пиримидины в ходе, зависимой от освещения, реакции. Фотолиаза предпочтительно репарирует CPD в линкетной ДНК. Репарация в нуклеосомах замедлена и, предположительно, облегчается динамическими свойствами нуклеосом, перемещающих повреждения ДНК в область линкерной ДНК.
Класс CDP-специфичных фотолиаз из микроорганизмов, определенный как класс I фотолиаз, был первым охарактеризованным представителем семейства фотолиаз. Близкородственный класс фотолиаз специфичных к 6-4-фотопродуктам был обнаружен недавно, представители этого семейства были найдены в Drosophila melanogaster, Xenopus laevis и Arabidopsis thaliana. Криптохромы, являющиеся фоторецепторами на фиолетовую часть светового спектра обнаруженные в растениях и других организмах, также являются близкородственными классу I фотолиаз.
Более дальнородственным семейством CPD-фотолиаз, названное классом II фотолиаз было идентифицировано в ряде видов, включая животных, Archaebacterium, Eubacterium и высших растений. Было показано, что все охарактеризованные фотолиазы содержат восстановленный FAD и большинство содержат вторичные хромофоры в зависимости от вида либо MTHF, либо 8-HDF. Подобный механизм реакции был предложен для обоих классов CPD-фотолиаз. Хромофор MTHF или 8-HDF подобен антенне, которая абсорбирует фиолетовый свет и расходует поглощенную энергию на регенерацию FADH-.
Состав кофактора растительной фотолиазы не до конца исследован, хотя, недавно было показано, что CPD-фотолиазы из Arabidopsis содержавшие только FADH обладали ферментативной активностью.
» Fritz Thoma, Light and dark in chromatin repair: repair of UV-induced DNA lesions by photolyase and nucleotide excision repair, Institut fur Zellbiologie, ETH-Zurich, Honggerberg, CH-8093 Zurich, Switzerland
» Characterization of Arabidopsis photolyase enzymes and analysis of their role in protection from ultraviolet-B radiation, Wanda M. Waterworth 1, Qing Jiang, Christopher E. West, M. Nikaido and Clifford M. Bray
Эксцизионная репарация
BER - эксцизионная репарация ДНК путем удаления поврежденных азотистых оснований.
Система BER вызывает защиту геномной ДНК от повреждений, вызываемых главным образом алкилирующими агентами, а также эндогенными генотоксическими соединениями, включая внутриклеточные радикалы кислорода и другие реакционноспособные метаболиты.
ДНК-гликозилазы - ключевые ферменты отщепляющие различные модифицированные основания ДНК с образованием АР-сайта.
АР-дезоксирибоза (apurinic/apyrimidinic deoxyribose), образовавшаяся в результате удаления модифицированного азотистого основания апуринового/апиримидинового (AP-) сайта, далее вырезается с помощью АР-лиазы, которая освобождает ее 3’-конец, и АР-эндонуклеазы, гидролизующей ее 5’-концевую фосфодиэфирную связь в АР-сайте.
Однонуклеотидная брешь затем заполняется с помощью ДНК-полимеразы, и фосфодиэфирная связь восстанавливается в реакции лигирования. У E. coli репаративный синтез ДНК выполняет ДНК-полимераза I, у дрожжей – ДНК- полимераза ?. Из трех ДНК-лигаз, которыми обладают клетки животных, в BER, по-видимому, участвует ДНК-лигаза III.
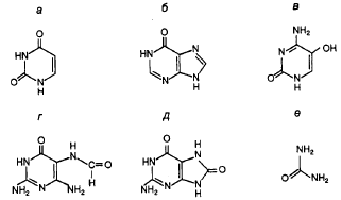
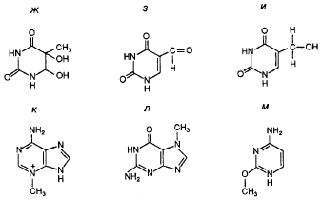
рис.1 Модифицированные азотистые основания ДНК, удаляемые ДНК–гликозилазами: а – урацил; б – гипоксантин; в – 5–гидроксицитозин; г – 2,5-диамино-4-формамидопиримидин; д – 7,8-дигидро-8-оксогуанин; е – мочевина; ж – тимингликоль; з – 5-формилурацил; и – 5-гидроксиметилурацил; к – 3-метиладенин; л – 7-метилгуанин; м – 2-метилцитозин [Партушев, 2000].
АP-эндонуклеаза создает ник (одноцепочечный разрав) с 3’-ОН и 5’-dRP концами. Для большинства млекопитающих характерен
тип BER репарации с включением одного нуклеотида. В этом случае ДНК-полимераза β вставляет 1 нуклеотид в 3’-конец праймера и затем удаляет 5’-dRP фрагмент с помощью своей dRP-лиазной активности. Получившийся ник сшивается ДНК-лигазой. Альтернативным является путь так называемой длинно-заплаточной BER репарации. Он реализуется в тех случаях, когда 5’-dRP фрагмент модифицирован и не может быть удален с помощью ДНК–полимеразы β. В этом случае Pol β проводит синтез ДНК с вытеснением запирающей цепи, 2 - 13 нуклеотидов. Образующийся в результате свисающий 5’-конец ДНК выщепляется флэпэндонуклеазой FEN1. Pol бета, Pol дельтаи Pol епсилон могут вести ситнез ДНК во время длинно-заплаточной репарации. Идентичность полимераз, вовлеченных в этот процесс in vitro, еще не ясна, но показано, что Pol β всегда инициирует синтез ДНК.
Зависимость того, какой из путей BER реализуется, определяется бифункциональными ДНК-гликозилазами, которые имеют дополнительную
АP-лиазную активность. При комбинации ДНК-гликозилазной, АP-лиазной и АP-эндонуклеазной активностей внутри одного фермента в поврежденной цепи ДНК образуется однонуклеотидная брешь с 3’-ОН и 5’-P концами, которую может застроить Pol β.
Дополнительная сложность в понимании механизмов переключения внутри BER состоит в том, что две новые полимеразы Pol i и Pol лямбда также имеют dRP-лиазнуюактивность. Таким образом, можно предположить, что они, как и Pol бета, являются участниками тех процессов репарации, где необходимо выщепление dRP фрагмента. Pol лямбда является близким гомологом Pol бета со сходными ферментативными свойствами. Также как и Pol бета, она лишена 3’-->5’экзонуклеазной активности и имеет низкую процессивность синтеза на частичном ДНК-дуплексе, содержащем свисающий 5’-участок матрицы, процессивный синтез возможен в брешах с 5’-P концами. Таким образом, Pol лямбда является подходящим кандидатом для BER синтеза. Более того,
Pol лямбда заменяет Pol бета в реконструированных BER системах, репарирующих урацил-содержащие ДНК, iv vitro. Однако, клетки мышей Pol лямбда -/- не чувствительны к обработке перекисью или метилметансульфонатом, агентам, которые, помимо других типов повреждений, продуцируют АР-сайты и окисленные формы оснований. Отсюда можно заключить, что Pol лямбда не является необходимой для BER в клетках, где есть, Pol дельта и Pol епсилон. Интересно, что Pol лямбда может эффективно процессировать ДНК при очень низкой концентрации dNTP (около 1 мкМ), что может означать ее участие в любых клеточных процессах в фазе G0 при низкой концентрации dNTP. В поддержку этой гипотезы выступает тот факт, что экспрессия Pol лямбда зависит от клеточного цикла, и наибольшее количества белка экспрессируется при переходе из S- в М-фазу и в спокойных клетках.
Pol i принадлежит к Y семейству полимераз. Основная функция полимераз этого семейства – утилизация ДНК-повреждений, блокирующих работу репликативных ДНК-полимераз. Однако,
исходя из некоторых свойств Pol i, можно предположить, что этот фермент является участником альтернативного процесса BER репарации. Pol i обладает низкой поцессивностью, лишена 3’>5’экзонуклеазной активности и способна застраивать брешь в 1 - 5 нуклеотидов iv vitro. Pol i может замещать Pol бета в реконструированных системах BER, репарирующих урацил-содержащие ДНК, iv vitro, благодаря наличию dRP-лиазной и ДНК-полимеразной активностей. Кинетические исследования реакции нуклеотидного встраивания овыявили дополнительные данные, свидетельствующие в пользу того, что Pol i может принимать участие в репарации. Pol i вставляет dTMP напротив А в ДНК-матрицу с большей эффективностью, чем любой другой дезоксинуклеозидмонофосфат, при этом точность ДНК-синтеза сопоставима с параметрами для Pol бета. Основываясь на этих данных, можно предположить, что Pol i – участник BER репарации оснований уридина, который образуется после встраивания dUMP напротив А во время ошибочной репликации. Pol i также
может вставлять dGМP напротив Т со скоростями, близкими к скорости включения корректного нуклеотида. Более того, на матрице, содержащей 2 или более последовательных Т, вторым встраиваемым нуклеотидом оказался dGMP. Подобные результаты служат основой для гипотезы, что Pol i может быть участником альтернативной BER репарации в тех слсучаях, когда dG был ошибочно удален гликозилазой из G-T или G-U некомплементарной пары, образовавшейся в результате дезаминации 5-метилцитозина или цитозина. Возможная роль Pol i в трансляции синтеза ДНК и процессе соматических гипермутаций рассмотрена ниже.
Возможность участия пяти ядерных полимераз в BER, три из которых обладают dRP-лиазной активностью, была мало изучена в клетках и на модельных животных, лишенных более чем одной полимеразы. Поэтому данные о субстратной специфичности и взаимодействии полимеразо-акцепторных белков, необходимых в BER, недостаточны. Помимо BER репарации, Pol бетта принимает участие в репарации одноцепочечных разрывов; функционирование
этого процесса нарушено у пациентов с наследственной спинномозговой атаксией. Одноцепочечные разрывы генерируются эндогенными или экзогенными агентами. Такие разрывы часто содержат однонуклеотидные бреши с 3’ и/или 5’ модифицированными концами, то есть очень похожи на субстраты BER. Так вот, интересно посмотреть, способны ли другие полимеразы с подобным набором исходных данных (Pol i и Pol лямбда) принимать участие в репарации одноцепочечных разрывов.
Четвертой ДНК-полимеразой в клетках человека, обладающей dRP-лиазной активностью, является митохондриальная ДНК-полимераза гамма. Pol гамма – единственная ДНК-полимераза, обнаруженная в митохондриях, следовательно, она ответственна за все преобразованиях ДНК, происходящие в этой органелле. Митохондрия является объектом интенсивного повреждения ДНК активными формами кислорода, генерируемыми во время окислительного фосфорилирования. Эти повреждения эффективно репарируются набором митохондриальных белков, которые включают в себя АP-эндонуклеазу, Pol гамма,
мтДНК-лигазу. Сам процесс репарации сходен с однонуклеотидным процессом BER в ядерной ДНК.
Таблица. ДНК-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в BER.
| Фермент | Источник | Ген | Субстрат (рис.1) |
| Урацил-ДНК-гликозилаза | E. coli S. cerevisiae Человек |
ung UNG UDG |
а а а |
| 3-Метиладенин-ДНК-гликозилаза | E. coli E. coli S. cerevisiae Человек |
tag alkA MAG MPG |
к з, к–м, (б, и) б, к, л к, (д) |
| Fapy/8-оксогуанин-ДНК- гликозилаза | E. coli S. cerevisiae |
fpg/mutM ? |
в–д г и/или д |
| (fapy – формамидопиримидин) | Человек | ? | г и/или д |
| Эндонуклеаза III/тимингликоль-ДНК-гликозилаза | E. coli | nth | в, е, ж |
| Эндонуклеаза VIII | E. coli | nei | в, е, ж |
| A-G-ДНК-гликозилаза | E. coli Человек |
mutY ? |
Аденин/в |
| G-T-ДНК-гликозилаза | Человек | ? | G-T, (U-G) |
| УФ-эндонуклеаза | T4 M. luteus |
? ? |
Пиримидиновые димеры |
| Гидроксиметилурацил-ДНК- гликозилаза | Человек | ? | з |
| Формилурацил-ДНК-гликозилаза | Человек | ? | ж |
NER - эксцизионная репарация ДНК путем удаления нуклеотидов.
При NER репарации поврежденные азотистые основания вырезаются в составе олигонуклеотидов, в отличии от BER, где происходит удаление отдельных поврежденных
азотистых оснований ДНК путем разрыва соответствующих N-гликозидных связей между азотистыми основаниями и остатками дезоксирибозы.
пути осуществления NER:
- Гидролиз фосфодиэфирной связи по 3’- или 5’-концу на некотором расстоянии от ошибочно спаренного (поврежденного) нуклеотида, который далее целиком удаляется под действием 5’-->3’- (или 3’-->5’-) экзонуклеазы, гидролизующей цепь ДНК нуклеотид за нуклеотидом в соответствующем направлении от первоначального одноцепочечного разрыва в репарируемой ДНК. Образующаяся брешь далее заполняется ДНК-полимеразой. Такой механизм репарации реализуется у E. coli и человека для вырезания неповрежденных (немодифицированных) ошибочно спаренных нуклеотидов. Механизм последовательного эндо- и экзонуклеазного расщепления ДНК не используется для удаления поврежденных (измененных) нуклеотидов. Это связано, по- видимому, с тем, что такие нуклеотиды (например возникшие в результате образования аддуктов с мутагенами) часто
являются ингибиторами экзонуклеаз - Одним из решений данной проблемы представляется использование ферментной системы, которая вносила бы одноцепочечные разрывы по обе стороны от поврежденного нуклеотида на некотором расстоянии от него с последующим удалением одноцепочечного фрагмента ДНК, содержащего измененный нуклеотид. Действительно, такой второй механизм эксцизионной репарации функционирует у всех исследованных видов живых организмов и будет рассмотрен ниже более подробно
В универсальном механизме эксцизионной репарации как прокариоты, так и эукариоты гидролизуют 3–5-ю фосфодиэфирную связь с 3'-конца отповреждения. При этом прокариоты гидролизуют также 8-ю связьот 5’-конца измененного нуклеотида, тогда как у эукариотических организмовпроисходит одноцепочечный разрыв на расстоянии 21–25 нуклеотидов отповреждения со стороны его 5’-конца. Таким образом, прокариоты удаляютизмененный нуклеотид в составе 12–13-членных олигомеров, тогда как
эукариоты – в составе одноцепочечных фрагментов ДНК длиной в 27–29 нуклеотидов. Ферментная система, вносящая такие двойные одноцепочечные
разрывы, получила название эксцизионной нуклеазы (эксцинуклеазы). Образующаяся в молекуле репарируемой ДНК одноцепочечная брешь далее заполняется с помощью ДНК-полимеразы, а фосфодиэфирная связь в остающемся одноцепочечном разрыве восстанавливается ДНК-лигазой.
NER устраняет ДНК-повреждения посредством вырезания олигонуклеотида, содержащего это повреждение, с образованием бреши в ДНК размером ~ 30 нуклеотидов. Эта брешь застраивается одной или двумя полимеразами В семейства Pol дельта или Pol епсилон. Любая из этих ДНК-полимераз способна застраивать подобную брешь в реконструированной системе, содержащей очищенные белки млекопитающих, in vitro. При изучении NER в системе фибробластов человека с нарушенной проницаемостью и в ядерном экстракте HeLa клеток обнаружили, что обе полимеразы необходимы для восстановления ДНК после УФ-облучения. Исследования
в дрожжевых системах показали, что та или другая ДНК-полимераза существенно дополняют репарацию УФ-поврежденной ДНК. Более поздние исследования показали, что оба фермента необходимы для эффективной NER репарации в дрожжевых экстрактах. Pol дельта и Pol епсилон способны вести процессивный синтез ДНК при наличии дополнительного фактора PCNA, который «надевается» на ДНК с помощью пятисубъединичного комплекса RFC. Репарационный синтез как Pol дельта, так и Pol епсилон также требует присутствия этих факторов процессивности.
Эксцизионная репарация нуклеотидов: введение
ЭР - эксцизионная репарация ДНК; ЭР-комплекс включает ПАРП , XRCC1 , ДНК-лигазу III и ДНК-полимеразу бета .
Два пути осуществления NER:
1. Гидролиз фосфодиэфирной связи по 3'- или 5'- концу на некотором расстоянии от ошибочно спаренного (поврежденного) нуклеотида, который далее целиком удаляется под действием 5'->3'- (или 3'->5'-) экзонуклеазы, гидролизующей
цепь ДНК нуклеотид за нуклеотидом в соответствующем направлении от первоначального одноцепочечного разрыва в репарируемой ДНК. Образующаяся брешь далее заполняется ДНК-полимеразой. Такой механизм репарации реализуется у E. coli и человека для вырезания неповрежденных (немодифицированных) ошибочно спаренных нуклеотидов. Механизм последовательного эндо- и экзонуклеазного расщепления ДНК не используется для удаления поврежденных (измененных) нуклеотидов. Это связано с тем, что такие нуклеотиды часто являются ингибиторами экзонуклеаз.
2. Функционирует у всех исследованных видов организмов и заключается в использовании ферментной системы, которая вносит одноцепочечные разрывы по обе стороны от поврежденного нуклеотида на некотором расстоянии от него с последующим удалением одноцепочечного фрагмента ДНК, содержащего измененный нуклеотид.
Гидролизуется 3-5-фосфодиэфирную связь с 3'-конца от повреждения. При этом прокариоты гидролизуют также 8-связь от 5'-конца
измененного нуклеотида, тогда как у эукариотических организмов происходит одноцепочечный разрыв на расстоянии 21-25 нуклеотидов от повреждения со стороны его 5'-конца. Таким образом, прокариоты удаляют измененный нуклеотид в составе 12-13-членных олигомеров, тогда как эукариоты - в составе одноцепочечных фрагментов ДНК длиной в 27-29 нуклеотидов. Ферментная система, вносящая такие двойные одноцепочечные разрывы, получила название эксцизионной нуклеазы (эксцинуклеазы) . Образующаяся в молекуле репарируемой ДНК одноцепочечная брешь далее заполняется с помощью ДНК-полимеразы, а фосфодиэфирная связь в остающемся одноцепочечном разрыве восстанавливается ДНК-лигазой.
В отличие от ЭРО и прямых реверсий, которые специфичны к достаточно узкому кругу повреждений ДНК, система ЭРН, хотя и с разной эффективностью, удаляет все возможные повреждения, и потому роль ее в поддержании стабильности генома велика. ЭРН детально изучена у E. coli и активно изучается в клетках
дрожжей и человека, причем в последних благодаря раскрытию генетической природы таких заболеваний, как пигментная ксеродерма ( ХР ), синдром Кокейна ( СS ) и заболевания трихотиодистрофия ( ТТD)
В ЭРН задействовано 6-8 генов у E. coli и до 30 у человека.
Если повреждение в транскрибируемой (матричной) нити ДНК задерживает продвижение РНК-полимеразы, то специальный белковый фактор TRCF ( transcription-repair coupling factor ) сталкивает РНК-полимеразу и связывает с этим местом комплекс ферментов репарации. См. Сопряжение транскрипции и репарации ДНК у E/coli.
Ферментный ансамбль осуществляющий первые 3 стадии процесса NER называется эксцинуклеазой.
В системе эксцизионной репарации ДНК путем удаления нуклеотидов поврежденные азотистые основания вырезаются в составе олигонуклеотидов.
NER: регуляция
Для клеток животных не характерен SOS-ответ, свойственный клеткам E. coli и представляющий собой суммарную реакцию бактериальной клетки на повреждение ДНК различными агентами,
проявляющийся в усилении транскрипции генов NER. Посттрансляционные модификации белков репарации, происходящие в ответ на повреждение ДНК, не влияют на активность эксцинуклеазы человека.
Обнаружено, что повреждения ДНК стабилизирует белок р53- белок-супрессор опухолевого роста, являющийся регулятором транскрипции. Имеются данные о том, что белок р53 может взаимодействовать с белками XPB и RPA, необходимыми для NER. Однако клетки с инактивированными генами р53 (p53(-/-)), как и клетки дикого типа, эффективно удаляют из поврежденной ДНК два основных фотопродукта, возникающих под действием УФ-света, и обладают такой же устойчивостью к УФ. Поэтому считается, что белок р53 не оказывает прямого влияния на NER. Белки Cdk7 и циклин H, которые образуют Cdk-активирующую киназу, входят в состав комплекса TFIIH, что позволяет предполагать наличие связи репарации ДНК с фазами клеточного цикла.
ЭРН (NER): сопряжение с транскрипцией (ТЭРН)
Транскрибируемые последовательности нуклеотидов ДНК, особенно
в матричной цепи, репарируются с большей скоростью, чем нетранскрибируемые последовательности. В клетках больных с синдромом Кокайна не наблюдается такой асимметрии в репарации.
В клетках E. coli белковый фактор, кодируемый геном mfd и сопрягающий транскрипцию и репарацию, замещает остановившиеся перед повреждением молекулы РНК-полимеразы, что приводит к диссоциации транскрипционного комплекса. При этом он привлекает экзонуклеазный репаративный комплекс к поврежденному участку ДНК. См. Сопряжение транскрипции и репарации ДНК (ТЭРН) у E/coli
В клетках животных ген CSB кодирует белок с молекулярной массой 160 кДа, который содержит хеликазный домен и, возможно, выполняет те же функции, что и белок Mfd у E. coli . На основе поведения клеток с мутантными генами белков CSA и CSB разработана модель механизма, с помощью которого обеспечивается асимметричная репарация цепей ДНК. В соответствии с этой моделью РНК-полимераза II , остановившаяся в процессе транскрипции
перед поврежденным участком ДНК, распознается комплексом CSA-CSB и перемещается в сторону от повреждения без разрушения четвертичной структуры транскрипционного комплекса. Одновременно комплекс CSA-CSB привлекает компоненты репаративной системы XPA и TFIIH к месту повреждения ДНК и помогает сборке эксцинуклеазного комплекса. Нуклеотиды поврежденной цепи вырезаются, и брешь репарируется. После этого РНК-полимераза в составе транскрипционного комплекса продолжает транскрипцию.
NER: механизм
Процесс NER можно разделить на четыре этапа: а) распознавание поврежденного участка ДНК; б) двойное надрезание (инцизия) цепи ДНК по обеим сторонам поврежденного участка и его удаление (эксцизия); в) заполнение бреши в процессе репаративного синтеза; г) лигирование оставшегося одноцепочечного разрыва ДНК.
NER человека распознает и удаляет одиночные ошибочно спаренные нуклеотиды, а также петли длиной в 1-3 нуклеотида. NER человека способна различать цепи ДНК в случае распознавания поврежденных
нуклеотидов. Показано, что при наличии в ДНК димеров тимина циклобутанового типа вырезание нуклеотидов происходит исключительно из поврежденной цепи. Механизм такого распознавания в настоящее время неизвестен, как и молекулярный механизм узнавания самих поврежденных оснований. Система способна распознавать повреждения как сильно, так и слабо деформирующие вторичную структуру ДНК. При этом не обнаружена линейная зависимость между коэффициентом специфичности нуклеазы (kcat/km) и уровнем деформации двойной спирали ДНК. Показано, что в процессе распознавания участвуют белковые комплексы XPA/RPA, которые преимущественно связываются с поврежденной ДНК, и TFIIH, обладающий АTP-зависимой ДНК-расплетающей активностью. Последний взаимодействует с поврежденным участком ДНК и по аналогии с соответствующим механизмом у E. coli локально раскручивает ДНК, создавая основной преинцизионный комплекс с поврежденной ДНК.
Установлено, что три фермента репарации, обладающие узкой
субстратной специфичностью: ДНК-фотолиаза (удаление пиримидиновых димеров), урацилгликозилаза (удаление урацила из ДНК) и экзонуклеаза III (гидролиз ДНК в AP-сайтах), втягивают поврежденный участок из двойной спирали в полость фермента, что приводит кофактор или аминокислотные остатки активного центра этих ферментов в непосредственный контакт с расщепляемыми связями ДНК. Не исключено, что система эксцинуклеазы действует таким же образом.
Основные этапы функционирования NER, следующие за распознаванием поврежденного участка ДНК, представлены на рис. I.59. После связывания комплекса XPA-RPA с измененным участком ДНК, XPA взаимодействует с комплексом TFIIH, который создает преинцизионный комплекс, что сопряжено с гидролизом ATP. ATP-зависимое расплетание ДНК комплексом TFIIH подготавливает ее к взаимодействию с двумя XP-белками, обладающими нуклеазной активностью. XPG связывается с TFIIH и вносит одноцепочечный разрыв с 3'-конца повреждения. Аналогично комплекс ERCC1-XPF
взаимодействует с XPA в составе преинцизионного комплекса и способствует одноцепочечному разрыву с 5'-конца повреждения. Образование обоих разрывов является ATP-зависимым, и их расположение на ДНК высокоспецифично. Как правило, происходят разрывы 5-й и 24-й фосфодиэфирных связей соответственно от 3'- и 5'-концов поврежденных участков. Однако расположение точек разрывов может варьироваться.
Таким образом, в результате подобных одноцепочечных надрезов ДНК может освобождаться фрагмент длиной 24-32 нуклеотида с преобладанием фрагментов длиной 27-29 нуклеотидов. На расположение сайтов одноцепочечных разрывов влияют характер повреждения и последовательности нуклеотидов (контекст), окружающих поврежденный участок. Ту же самую картину инцизии обнаруживают in vivo в ооцитах Xenopus и у Schizosaccharomyces pombe. На этом основании делают вывод об универсальном механизме эксцизионной репарации у эукариот.
Репаративный синтез ДНК у человека является PCNA-зависимым,
т.е. может осуществляться с участием ДНК-полимераз Polдельта и Polэпсилон. PCNA связывается с системой праймер-матрица под действием фактора репликации RFC, откуда следует, что последний также участвует в репаративном синтезе ДНК. В опытах с бесклеточными системами моноклональные антитела к Polдельта специфически подавляют репаративный синтез. Однако оказалось, что в тех же высокоочищенных бесклеточных системах вместо Polдельта с аналогичным эффектом могут быть использованы Polэпсилон и даже фрагмент Кленова ДНК-полимеразы I E. coli. Это означает, что реконструированные из очищенных компонентов бесклеточные системы лишь в ограниченной степени имитируют биохимические процессы, происходящие в живых клетках. Считается, что обе ДНК-полимеразы - Polдельта и Polэпсилон участвуют в репаративном синтезе ДНК у человека.
ПАРП: модели управления процессом эксцизионной репарации ДНК
ПАРП - один из первых ядерных факторов, распознающих повреждение ДНК , и поэтому в идеальном случае управляет запуском механизма
репарации ДНК в живых клетках с места повреждения ДНК. Эта модель поддерживается идентификацией ЭР -комплекса, включающего ПАРП , XRCC1 , ДНК-лигазу III и ДНК-полимеразу бета . Присутствие ПАРП в таком мультипротеиновом комплексе доказывает, что этот фермент может направлять аппарат репарации ДНК к сайтам повреждения ДНК in vivo и облегчает осуществление репарации по этому пути.
XRCC1-белок действует как молекулярные "леса", формируя ЭР-комплекс путем индивидуального взаимодействия с каждым компонентом. С тех пор, как была обнаружена возможность поли(АДФ-рибозил)ирования XRCC1-белка in vitro, можно предположить, что ПАРП способен регулировать активность комплекса путем модифицирования XRCC1-белка in vivo и нарушать его способность взаимодействовать с другими компонентами комплекса. Было показано, что сверхэкспрессия XRCC1-белка подавляет активность ПАРП в живых клетках.
Аналогично ДНК-лигаза III ингибирует активность ПАРП in vitro, когда ее количества превышают количества ПАРП.
ПАРП может также рекрутировать факторы репарации ДНК путем модификации хроматиновых белков. Длинные цепи ПАР действительно способны направить ферменты репарации к сайтам разрывов ДНК значительно быстрее, нежели если они ищут повреждение сами по всему ядру. Такая модель согласуется с активностью ПАРП перед и/или после удаления поврежденных оснований.
NER: структура и функции белков
В табл. I.21 суммированы свойства белков животных, участвующих в NER. Большинство этих белков существует in vivo в виде комплексов, поэтому ферментативные активности, обнаруживаемые у отдельных белков в очищенном состоянии, могут не иметь прямого отношения к их функциям в системе NER.
XPA - белок с молекулярной массой 31 кДа, обладает доменом типа "цинковые пальцы", участвует в распознавании поврежденного участка ДНК, взаимодействует с другими компонентами системы и может функционировать в качестве фактора нуклеации для экзонуклеазы. XPA взаимодействует своим N-концевым доменом
с гетеродимером ERCC1-XPF, а С-концевым доменом - с TFIIH.
Белок RPA (HSSB) образует комплекс с XPA и усиливает его специфичность в отношении поврежденной ДНК. RPA (HSSB) - тример, состоящий из белковых субъединиц р70, р34 и р11, необходим для репликации ДНК и репаративного синтеза, а также для прохождения этапа двойного надреза ДНК во время эксцизионной репарации. Он обладает умеренным сродством к поврежденной ДНК.
TFIIH - олигомерный комплекс, в состав которого входят белки р89, р80, р62, р44, р41, р38 и р34. Этот белковый комплекс был открыт как один из семи основных факторов транскрипции, необходимых для эффективного функционирования РНК-полимеразы II . Субъединица р89 идентична белку репаративного комплекса XPB. Обнаружено отсутствие функциональной комплементации между бесклеточными экстрактами клеток с мутантными белками XPB и XPD, определяемой по восстановлению репарирующей активности в смешанных экстрактах. Комплекс TFIIH представляет собой
фактор репаративной системы. Белки XPB и XPD являются ДНК-зависимыми АТРазами, обладают хеликазными доменами и могут (как и сам фактор TFIIH) вызывать диссоциацию гибридов, образованных между короткими фрагментами ДНК и одноцепочечной ДНК.
XPC - белок с молекулярной массой около 125 кДа, существует в виде гетеродимера в комплексе с белком р58, который является гомологом белка Rad23 дрожжей (HHR23B). XPC слабо связывается с TFIIH и очень прочно - с одноцепочечной ДНК.
ERCC1/XPF - прочный белковый комплекс, с которым взаимодействует белок XPA, обладающий эндонуклеазной активностью, специфичной в отношении одноцепочечной ДНК.
XPG - белковый комплекс, обладающий эндонуклеазной активностью, специфичной в отношении одноцепочечной ДНК; вовлекается в эксцизионный комплекс посредством взаимодействия с TFIIH и RPA.
ЭРН (NER): генетика
Гены NER E. coli, uvrA, uvrB и uvrC не обнаруживают гомологии с соответствующими генами человека. Гены NER дрожжей и человека
высокогомологичны, и энзимология эксцизионной репарации также обладает большим сходством. По крайней мере, три заболевания у человека вызываются генетическими нарушениями системы эксцизионной репарации: пигментная ксеродерма, синдром Кокейна и трихотиодистрофия.
Кожа больных пигментной ксеродермой обладает повышенной чувствительностью к дневному свету, что проявляется в виде фотодерматозов, включая рак кожи. В ряде случаев отмечены аномалии нервной системы, причиной которых являются мутации в одном из семи генов: XPA, XPB, XPC, XPD, XPE, XPF, XPG. Однако описаны больные с классическими симптомами пигментной ксеродермы, но с ненарушенной системой NER. Для клеток этих больных характерны изменения в так называемой пострепликативной репарации .
Больным с синдромом Кокейна присущи нарушения роста, умственная отсталость, катаракты, повышенная чувствительность к свету с сопутствующими дерматозами. Обнаружены мутации в двух группах генов, приводящие к этому заболеванию. У больных
с мутантными генами CS-A или CS-B клетки способны нормально репарировать УФ-повреждения ДНК. У другой группы больных обнаружены мутации в генах XPB, XPD или XPG.
У больных трихотиодистрофией со смешанными симптомами выявлены мутации в генах XPB или XPD. Классические симптомы этого заболевания, по-видимому, являются следствием мутации в гене транскрипционного фактора TFIIH.
Получение мутантов с измененной NER у грызунов позволило разбить такие гены на 11 групп комплементации, большинство из которых соответствует группам комплементации XP и CS человека. Часть соответствующих генов человека удалось клонировать, используя их способность исправлять (комплементировать) генетические дефекты в культивируемых мутантных клетках грызунов. Эти гены получили название кросс-комплементирующих генов эксцизионной репарации ( ERCC - excision repair cross complementing ). Среди них гены XPE и ERCC6-ERCC11 не требовались для прохождения основных реакций эксцизионной репарации, и их функция неизвестна.
Эксцизионная репарация нуклеотидов (ЭРН) E. coli
У E. coli эксцинуклеаза формируется, в результате димеризации двух молекул белка UvrА в присутствии АТР и связывания с одной молекулой UvrB. Гетеротример UvrA2B связывается с ДНК и с помощью 5'-3'-ДНК-геликазной активности перемещается вдоль ДНК в поисках повреждения. Такова предполагаемая картина узнавания эксцинуклеазой UvrAВС неспецифического повреждения в ДНК [ Hoeijmakers J., 1993 ]. Результатом узнавания повреждения этим комплексом явится внедрение субъединицы UvrB в ДНК, сопровождающееся конформационными изменениями ДНК в сайте внедрения ( изломы , локальная денатурация), диссоциация обеих субъединиц UvrА из комплекса и последующее связывание с ним молекул UvrD и UvrC. Гетеродимер UvrBC из состава нового комплекса делает два разрыва в поврежденной нити ДНК на расстоянии 8 н. с 5'-конца от повреждения и 5 н. с 3'-конца, катализируемых субъединицами UvrC и UvrB соответственно, что приводит к появлению 12-13-мерного олигонуклеотида,
вытесняемого из комплекса с помощью геликазы UvrD. Образующаяся при этом брешь заполняется ДНК-полимеразой I, синтезирующей ДНК по неповрежденной матрице, и сшивается ДНК-лигазой. Описанный процесс зависит от АТР. Действительно, АТР стимулирует димеризацию молекул UvrA, гидролиз АТР необходим для образования комплекса UvrA2B и проявления его геликазной активности, АТР необходим для формирования комплекса UvrB-ДНК и, наконец, для описанной выше бимодальной инцизии ДНК [ Friedberg E.C., Walker G.C., ea., 1991 ]. У E. coli транскрипционно-зависимую ветвь ЭРН (ТЭРН) осуществляет продукт гена mfd (mutation frequency decline). Этот ген был открыт за 35 лет до того, как его продукт признали фактором TRCF. Последний способствует диссоциации РНК-полимеразы от дефектной транскрибируемой нити ДНК, и связывается с субъединицей UvrA эксцинуклеазного комплекса. Иными словами, именно белок Mfd отыскивает повреждения на транскрибируемой нити и направляет ТЭРН на эту мишень.
Согласно недавним наблюдениям, два главных белка системы ДКНО - MutL и MutS - необходимы для ТЭРН [106 Melon I., Champl G.N., 1996106]. Причина такой взаимосвязи систем ДКНО и ТЭРН или заимствования белков MutL и MutS для выполнения сходных функций пока остается загадочной, хотя сам факт несомненен и нашел подтверждение также и для белков Msh2, Mlh1, Pms1 и Msh3 у S. cerevisiae [ Sweder K.S., ea, 1996 ].
Эксцизионная репарация нуклеотидов (ЭРН) у человека
Большому прогрессу в раскрытии механизма ЭРН у эукариот мы обязаны наследственному заболеванию человека - пигментной ксеродерме .
Изучение молекулярных основ этого заболевания выявили их сопряженность с дефектами системы ЭРН, результатом чего и явилось раскрытие генетического контроля ЭРН. Комплементационный анализ различных клеточных линий ХР определил 8 комплементационных групп (7 от XPA до XPG и одна "вариантная форма" XPV) [ Friedberg E.C., Walker G.C., ea., 1991 ]), а комплементационная
коррекция возможных мутантных линий клеток китайского хомячка, чувствительных к УФ-свету, способствовала выявлению дополнительных генов системы ЭРН. Последние получили название гены ERCC (excision repair cross-complimenting), и поэтому в названии генов и белков ЭРН используются обе аббревиатуры. Хотя детали процесса ЭРН у человека не ясны, так как не определена роль целого ряда генов, в первом приближении он выглядит так ( табл. 3 ) [ Lehmann A.R., 1995 , Lindahl T., ea, 1997 , Hoeijmakers J., 1993 ]. Белок ХРА в комплексе с онДНК-связующим белком RPA ( репликационным белком А ), транслоцируясь вдоль онДНК, опознает конформационнoе повреждениe. Взаимодействуя через другой участок белка ХРА с базальным фактором транскрипции TFIIH (две из субъединиц которого, белки ХРВ и ХРD , обладают геликазной активностью с противоположной ориентацией раскручивания днДНК), они образуют комплекс, который расплетает ДНК вокруг повреждения (в состав этого комплекса входит и белок ХРС
с неясными функциями). Через третий участок белка ХРА к комплексу примыкает гетеродимер ERCC1-XPF , который вносит однонитевой разрыв в ДНК с 5'-конца на расстоянии 16-25 н. от повреждения, тогда как белок XPG , входящий в комплекс белков эксцинуклеазы через взаимодействие с белком RPA, делает надрез с 3'-конца на расстоянии 2-9 н. (в разрезании принимает участие и белок ХРС , а белок ХРЕ активирует реакцию). В результате бимодальной инцизии участок ДНК размером около 29 н. высвобождается, а образующаяся брешь ресинтезируется с помощью ДНК-полимеразы епсилон или ДНК-полимеразы дельта , сопутствующего репликации фактора PCNА , репликационного фактора C-RFС и ДНК-лигазы I .
Представленная картина во многом основана на реконструировании процесса в открытой системе с участием 10 хорошо очищенных белков [ Wood R.D., 1994 ]. Как видно, эукариотическая система ЭРН лишь функционально подобна прокариотической. В ней задействовано значительно больше белков, число которых должно еще возрасти
за счет белков, осуществляющих разборку и сборку хроматина. Раскрытие природы ТЭРН у человека также связывают с пониманием молекулярного дефекта,приводящего к развитию двух мультисистемных генетических заболеваний - синдрома Кокейна (СS) и трихотиодистрофии ( ТТD ). При обоих заболеваниях соматические клетки больных оказались неспособны к ТЭРН. Классические случаи CS оказались связанными с повреждениями в двух генах, CSA и CSB, а редкие смешанные формы CS+XP (CS с дополнительными симптомами ХР), с повреждениями в генах ХРВ, ХРD и ХРG. При ТТD дефекты были обнаружены также в генах XPB и XPD и в новом пока не клонированном гене ТТDА, продукт которого является частью корового домена транскрипционного фактора TFIIH [ Lehmann A.R., 1995 , Lindahl T., ea, 1997 ].
Фактор TFIIH состоит из 6 субъединиц, две из которых - белки XPB и XPD. Связываясь с белками РНК-полимеразного комплекса, кор TFIIH принимает участие в инициировании транскрипции [ Buratowski S., 1994 ], a вкупе с белками репарационного
комплекса кор этого фактора участвует в ЭРН. Если допустить, что белки CSA и CSB способствуют превращению транскрипционного комплекса в репарационнный [ Lindahl T., ea, 1997 , Bregman D.B., 1996 ], то следствием повреждения этих белков может стать дефектность в ТЭРН. Таким образом, либо прямыми воздействиями на коровый домен фактора TFIIH (мутации в генах XPB, XPD и TTDA), либо косвенными (через гены CSA и CSB) можно модифицировать способность этого фактора к диссоциации из РНК- полимеразного комплекса для участия в ТЭРН. Что касается белка XPG, то он, подобно своему гомологу из S. cereivisiae - белку Rad2 [ Bregman D.B., 1996 ], способен взаимодействовать c TFIIH, что допускает возможность его воздействия на TFIIH для участия в ТЭРН. Таковы гипотетические объяснения взаимосвязи молекулярных дефектов при CS и ТTD с нарушениями ТЭРН, которые могут быть полезными для раскрытия механизма ТЭРН у эукариот. Связь же между молекулярными дефектами и клиническими проявлениями
рассматриваемых наследственных заболеваний пока не имеет даже упрощенных толкований [ Kolodner R., 1995 ].
Так случилось, что изучение молекулярных механизмов ЭРН и ТЭРН на клетках человека развивались параллельно, или даже опережая исследования на популярной эукариотической модели дрожжей S. cerevisiae. В табл. 3 представлены известные функциональные аналоги системы ЭРН у дрожжей. Несомненно, однако, что при исследовании детального механизма ЭРН именно эта модельная система будет играть ведущую роль. Например, немаловажной особенностью системы ЭРН у E. coli является ее связь с SOS-функциями клетки. Действительно, центральные гены системы ЭРН, uvrA и uvrB, находятся под контролем SOS-регулона [ Friedberg E.C., Walker G.C., ea., 1991 ]. Системы, подобной SOS, у эукариот пока не обнаружено. Однако целый ряд генов системы ЭРН у дрожжей, таких, как RAD2, RAD7, RAD23, CDC8 и CDC9, индуцируется при повреждении ДНК, а последние два гена дополнительно регулируются клеточным циклом [ Friedberg
E.C., Walker G.C., ea., 1991 ].
Природу этой индукции еще предстоит выяснить.